Small: Nanosensoren für den Nachweis von Kontaminanten in Lebensmitteln
Die Gewährleistung der Sicherheit und Qualität von verarbeiteten und primären Lebensmitteln ist eine globale Herausforderung. Auf Nanopartikeln basierende Sensoren bieten hier eine schnelle und kostengünstige Lösung für den Nachweis von Schadstoffen oder Krankheitserregern. In ihrem Beitrag für die Fachzeitschrift Small zeigen Forschende um Pierre Picchetti das Potenzial dieser Nanosensoren zum Nachweis gleich mehrerer Zielsubstanzen in Lebensmittelproben mit der erforderlichen Selektivität, Empfindlichkeit und Geschwindigkeit für eine Hochdurchsatzanalyse. Darüber hinaus ist diese Technologie robust, auch für nicht spezialisiertes Personal einfach zu handhaben und kann chemische Substanzen in allen Zuständen von flüssig bis fest bei extrem niedrigen Konzentrationen erkennen.
Mit seiner KIT-Nachwuchsgruppe am Institut für Nanotechnologie konzentriert sich Pierre Picchetti auf die Entwicklung synthetischer Nanomaterialien, die enzymatische Funktionen nachahmen, sowie auf Nanotransporter, die ihre Fracht gezielt und auf Abruf als Reaktion auf äußere Reize freisetzen können.
Nanozyme
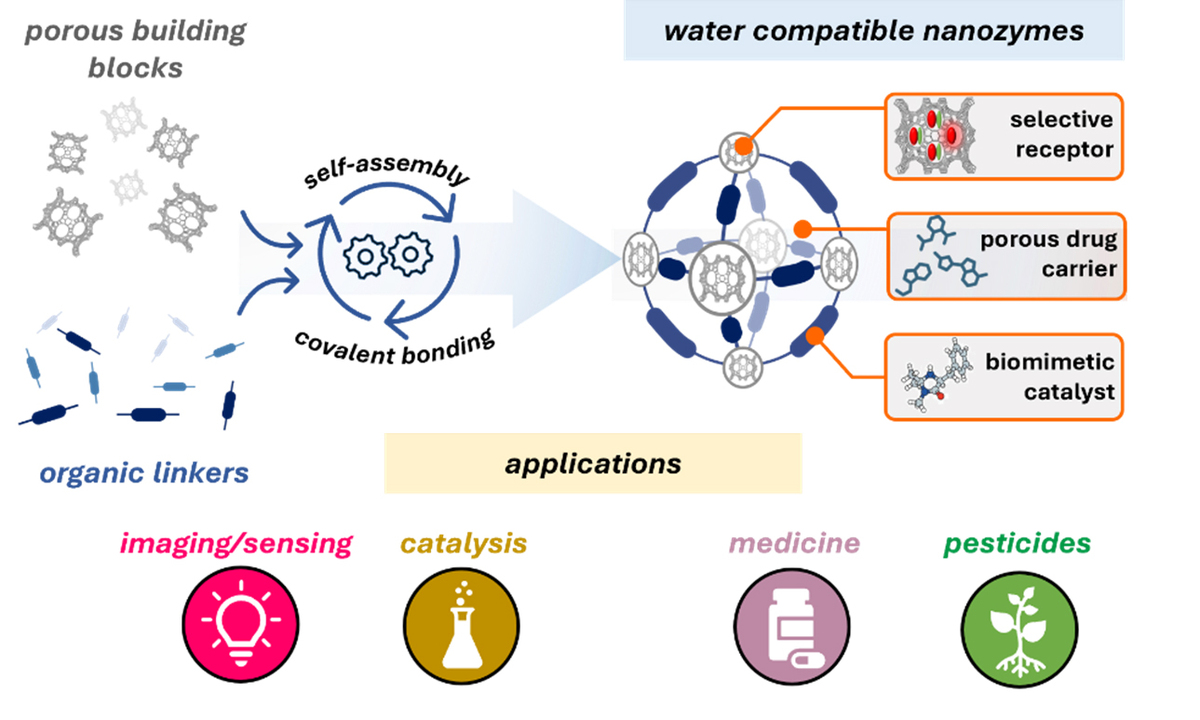
„Unser Ziel bei den Nano-Enzymen – kurz Nanozymen – ist es, zentrale Eigenschaften natürlicher Enzyme für Anwendungen in der Biosensorik, Katalyse oder Biomedizin nachzubilden“, erklärt Picchetti. „Meine Vision ist es, diese synthetischen Systeme als funktionale Äquivalente zu gestalten, die in der Lage sind, den Zellstoffwechsel mit hoher Präzision zu modulieren.“ Dieser Ansatz könnte den Weg für neue in situ-Therapien ebnen, bei denen der Wirkstoff direkt innerhalb der Zelle synthetisiert wird. Dadurch werden gezieltere und effektivere Behandlungen möglich – auch bei Krebs. Zu diesem Zweck verwenden die Forschenden biokompatibles Silica als Grundmaterial, dem sie präzise zusammengesetzte Bausteine hinzufügen. Diese Bausteine sind organische Gruppen, die besondere Funktionen erfüllen – wie Schlüssel für verschiedene Schlösser. Dadurch, dass sie nicht auf Proteinen basieren, verringert sich das Risiko einer Immunreaktion. Die Kombination aus supramolekularer und kovalenter Chemie ermöglicht zudem eine schnelle, kostengünstige und skalierbare Synthese stabiler Nanozyme. „Ein besonders vielversprechender Ansatz besteht darin, Nanozyme als intrazelluläre Katalysatoren zu entwickeln, die therapeutische Wirkstoffe als Reaktion auf äußere Reize erzeugen“, fährt Picchetti fort. Während dieser Ansatz im Prinzip bereits funktioniert, bestehen Herausforderungen bei der präzisen Zielansteuerung und der Reaktionsfähigkeit auf nicht-invasive äußere Reize wie zum Beispiel Ultraschall oder Infrarotlicht.
Nanotransporter
Die gezielte und zeitlich abgestimmte Freisetzung bioaktiver Substanzen in biologischen Systemen – etwa von Tieren oder Pflanzen – ist eine zentrale Herausforderung für die Entwicklung sicherer Therapien und Alternativen zu Pestiziden. Ein Beispiel ist der Covid-19-Impfstoff, bei dem eine Messenger-Ribonukleinsäure (mRNA) in ein lipidhaltiges Trägersystem eingebettet wird, um eine sofortige biologische Zersetzung nach der lokalen Injektion in einen Muskel zu verhindern. „Wir entwickeln anorganische Nanotransporter, die sowohl kosteneffizienter als auch chemisch robuster sind“, so Pierre Picchetti. „Eine Therapie ist deutlich wirksamer, wenn der Wirkstoff direkt in den Blutkreislauf verabreicht werden kann und somit die meisten Teile eines Organismus erreicht.“ Seine Nachwuchsgruppe verwendet Nukleinsäuren als programmierbare strukturelle Komponenten zur Herstellung hybrider organisch-anorganischer Materialien. Dadurch wird die Stabilität der Nukleinsäuren erhöht und gleichzeitig die Funktionalität der anorganischen Komponenten erweitert. Derzeit testen sie diese neuen Materialien für Anwendungen, die von reizempfindlichen Transportsystemen für mRNA-Therapien bis hin zu nukleinsäurebasierten Strategien zum Schutz von Nutzpflanzen reichen. In den Chemical Society Reviews diskutieren Forschende um Pierre Picchetti die Anwendung der supramolekularen Chemie in der Pflanzenwissenschaft und Landwirtschaft im Detail – darunter die In-vivo-Erfassung und -Überwachung von Pflanzenprozessen sowie die Herstellung sicherer und wirksamerer Pestizide.
Weitere Veröffentlichungen:
- P. Picchetti*, M. V. Balli, S. Baker, N. Manoj Kumar, P. Gruhs, L. Prodi, F. Biedermann*, Anal. Sens. 2024, 4, e202400025. DOI: 10.1002/anse.202400025
- P. Picchetti, S. Volpi, M. Sancho-Albero, M. Rossetti, M. D. Dore, T. Trinh, F. Biedermann, M. Neri, A. Bertucci, A. Porchetta*, R. Corradini*, H. Sleiman*, L. De Cola*, J. Am. Chem. Soc. 2023, 145, 22903-22912. DOI: 10.1021/jacs.3c04345
- N. Manoj Kumar, P. Gruhs, A. Casini, F. Biedermann, G. Moreno-Alcántar, P. Picchetti*, ACS Sens. 2023, 8, 2525-2532. DOI: 10.1021/acssensors.3c00008
- N. Manoj Kumar, P. Picchetti*, C. Hu, L. M. Grimm, F. Biedermann*, ACS Sens. 2022, 7, 2312-2319. DOI:10.1021/acssensors.2c00934
- P. Picchetti, G. Moreno-Alcántar*, L. Talamini, A. Mourgout, A. Aliprandi, L. De Cola*, J. Am. Chem. Soc. 2021, 143, 7681-7687. DOI: 10.1021/jacs.1c00444